Supporting information
Crystallographic Information File (CIF) https://doi.org/10.1107/S0108270104013162/dn1050sup1.cif | |
Structure factor file (CIF format) https://doi.org/10.1107/S0108270104013162/dn1050Isup2.hkl |
Le composé β-LiMoO2AsO4 a été préparé à partir de 0.12 g de Li2CO3, 1.07 g de NH4H2AsO4 et 0.94 g d'acide molybdique. Le mélange, finement broyé, est préchauffé à l'air, par palier de 100 K, jusqu'à 673 K en vue d'éliminer NH3, H2O et CO2. Le résidu final, refroidi puis broyé, est porté ensuite à 883 K où il est à l'état fondu. On baisse ensuite la température du four à moufle jusqu'à 868 K. Le mélange, à l'état pâteux pour favoriser la cristallization, est maintenu à cette température pendant 4 jours. Un refroidissement lent (5 K h−1) a été appliqué, jusqu'à 773 K, puis plus rapide (50 K h−1) jusqu'à la température ambiante. Des cristaux de couleur jaunâtre ont été séparés.
L'examen de la Fourier-différence finale revèle l'existence d'un pic residuel Q1 d'intensité maximale (ρmax = 1,38 e/Å3) situé à une distance de l'atome de molybdène Mo1 (Q1—Mo1 0,82 Å). L'absence d'un nombre suffisant de paires de Friedel n'a pas permis un affinement correct du paramètre de Flack et la structure absolue n'a pas pu être déterminée.
Data collection: CAD-4 EXPRESS (Duisenberg, 1992; Macíček & Yordanov, 1992); cell refinement: CAD-4 EXPRESS; data reduction: XCAD4 (Harms & Wocadlo, 1995); program(s) used to solve structure: SHELXS86 (Sheldrick, 1990); program(s) used to refine structure: SHELXL97 (Sheldrick, 1997); molecular graphics: DIAMOND (Brandenburg, 1998); software used to prepare material for publication: SHELXL97.
| LiMoO2(AsO4) | F(000) = 504 |
| Mr = 273.80 | Dx = 4.040 Mg m−3 |
| Monoclinic, P21 | Mo Kα radiation, λ = 0.71073 Å |
| Hall symbol: P 2yb | Cell parameters from 25 reflections |
| a = 5.1173 (7) Å | θ = 10–16° |
| b = 8.561 (2) Å | µ = 10.15 mm−1 |
| c = 10.309 (1) Å | T = 298 K |
| β = 94.63 (1)° | Prism, yellowish |
| V = 450.16 (13) Å3 | 0.16 × 0.08 × 0.04 mm |
| Z = 4 |
| Enraf-Nonius CAD-4 diffractometer | 1325 reflections with I > 2σ(I) |
| Radiation source: fine-focus sealed tube | Rint = 0.030 |
| Graphite monochromator | θmax = 30.0°, θmin = 3.1° |
| ω/2θ scans | h = −1→7 |
| Absorption correction: ψ scan (North et al., 1968) | k = 0→12 |
| Tmin = 0.343, Tmax = 0.676 | l = −14→14 |
| 1801 measured reflections | 2 standard reflections every 120 min |
| 1385 independent reflections | intensity decay: 1% |
| Refinement on F2 | Primary atom site location: structure-invariant direct methods |
| Least-squares matrix: full | Secondary atom site location: difference Fourier map |
| R[F2 > 2σ(F2)] = 0.025 | w = 1/[σ2(Fo2) + (0.036P)2] where P = (Fo2 + 2Fc2)/3 |
| wR(F2) = 0.064 | (Δ/σ)max < 0.001 |
| S = 1.09 | Δρmax = 1.38 e Å−3 |
| 1385 reflections | Δρmin = −1.72 e Å−3 |
| 164 parameters | Extinction correction: SHELXL97 (Sheldrick, 1997), Fc*=kFc[1+0.001xFc2λ3/sin(2θ)]-1/4 |
| 1 restraint | Extinction coefficient: 0.050 (2) |
| LiMoO2(AsO4) | V = 450.16 (13) Å3 |
| Mr = 273.80 | Z = 4 |
| Monoclinic, P21 | Mo Kα radiation |
| a = 5.1173 (7) Å | µ = 10.15 mm−1 |
| b = 8.561 (2) Å | T = 298 K |
| c = 10.309 (1) Å | 0.16 × 0.08 × 0.04 mm |
| β = 94.63 (1)° |
| Enraf-Nonius CAD-4 diffractometer | 1325 reflections with I > 2σ(I) |
| Absorption correction: ψ scan (North et al., 1968) | Rint = 0.030 |
| Tmin = 0.343, Tmax = 0.676 | 2 standard reflections every 120 min |
| 1801 measured reflections | intensity decay: 1% |
| 1385 independent reflections |
| R[F2 > 2σ(F2)] = 0.025 | 164 parameters |
| wR(F2) = 0.064 | 1 restraint |
| S = 1.09 | Δρmax = 1.38 e Å−3 |
| 1385 reflections | Δρmin = −1.72 e Å−3 |
Geometry. All e.s.d.'s (except the e.s.d. in the dihedral angle between two l.s. planes) are estimated using the full covariance matrix. The cell e.s.d.'s are taken into account individually in the estimation of e.s.d.'s in distances, angles and torsion angles; correlations between e.s.d.'s in cell parameters are only used when they are defined by crystal symmetry. An approximate (isotropic) treatment of cell e.s.d.'s is used for estimating e.s.d.'s involving l.s. planes. |
Refinement. Refinement of F2 against ALL reflections. The weighted R-factor wR and goodness of fit S are based on F2, conventional R-factors R are based on F, with F set to zero for negative F2. The threshold expression of F2 > σ(F2) is used only for calculating R-factors(gt) etc. and is not relevant to the choice of reflections for refinement. R-factors based on F2 are statistically about twice as large as those based on F, and R- factors based on ALL data will be even larger. |
| x | y | z | Uiso*/Ueq | ||
| As1 | 0.6178 (1) | 0.07722 (9) | 0.53570 (6) | 0.0065 (2) | |
| As2 | 1.1579 (1) | 0.19749 (8) | 0.89227 (6) | 0.0061 (2) | |
| Mo1 | 0.6783 (1) | −0.06862 (7) | 0.84352 (5) | 0.0071 (1) | |
| Mo2 | 0.8849 (1) | 0.42031 (7) | 0.66522 (5) | 0.0074 (1) | |
| Li1 | 0.321 (3) | −0.409 (2) | 0.904 (2) | 0.026 (4) | |
| Li2 | 0.955 (3) | −0.231 (2) | 0.605 (2) | 0.024 (3) | |
| O1 | 0.8199 (9) | −0.0645 (8) | 0.4926 (5) | 0.0123 (9) | |
| O2 | 0.755 (1) | 0.2552 (6) | 0.5163 (5) | 0.010 (1) | |
| O3 | 0.545 (1) | 0.0547 (7) | 0.6924 (5) | 0.012 (1) | |
| O4 | 0.320 (1) | 0.0793 (7) | 0.4487 (5) | 0.011 (1) | |
| O5 | 0.8699 (9) | 0.1357 (7) | 0.9379 (5) | 0.0101 (9) | |
| O6 | 1.388 (1) | 0.0628 (7) | 0.9319 (5) | 0.011 (1) | |
| O7 | 1.113 (1) | 0.2453 (6) | 0.7321 (5) | 0.009 (1) | |
| O8 | 1.233 (1) | 0.3684 (7) | 0.9684 (5) | 0.011 (1) | |
| O9 | 0.502 (1) | −0.2377 (7) | 0.8179 (5) | 0.014 (1) | |
| O10 | 0.963 (1) | −0.1131 (7) | 0.7745 (5) | 0.016 (1) | |
| O11 | 0.643 (1) | 0.3950 (7) | 0.7670 (6) | 0.016 (1) | |
| O12 | 1.069 (1) | 0.5691 (7) | 0.7368 (5) | 0.015 (1) |
| U11 | U22 | U33 | U12 | U13 | U23 | |
| As1 | 0.0078 (3) | 0.0067 (3) | 0.0051 (3) | −0.0003 (2) | 0.0017 (2) | −0.0003 (2) |
| As2 | 0.0065 (3) | 0.0064 (3) | 0.0054 (3) | 0.0004 (2) | 0.0011 (2) | −0.0003 (2) |
| Mo1 | 0.0084 (2) | 0.0075 (3) | 0.0056 (2) | 0.0003 (2) | 0.0016 (2) | −0.0004 (2) |
| Mo2 | 0.0087 (2) | 0.0077 (3) | 0.0058 (2) | −0.0001 (2) | 0.0006 (2) | 0.0000 (2) |
| Li1 | 0.035 (9) | 0.023 (8) | 0.019 (7) | −0.018 (7) | −0.002 (6) | 0.008 (7) |
| Li2 | 0.027 (8) | 0.009 (6) | 0.037 (9) | 0.007 (6) | 0.013 (6) | 0.005 (6) |
| O1 | 0.010 (2) | 0.017 (3) | 0.010 (2) | 0.008 (2) | 0.003 (2) | −0.002 (2) |
| O2 | 0.013 (2) | 0.008 (2) | 0.008 (2) | −0.004 (2) | 0.000 (2) | 0.002 (2) |
| O3 | 0.013 (2) | 0.017 (3) | 0.005 (2) | 0.002 (2) | 0.002 (2) | 0.004 (2) |
| O4 | 0.007 (2) | 0.013 (2) | 0.011 (2) | 0.000 (2) | −0.003 (2) | −0.001 (2) |
| O5 | 0.007 (2) | 0.011 (2) | 0.012 (2) | −0.001 (2) | 0.000 (2) | −0.003 (2) |
| O6 | 0.009 (2) | 0.014 (3) | 0.009 (2) | 0.003 (2) | −0.002 (2) | 0.001 (2) |
| O7 | 0.013 (2) | 0.008 (2) | 0.006 (2) | 0.004 (2) | 0.001 (2) | 0.003 (2) |
| O8 | 0.021 (2) | 0.006 (2) | 0.007 (2) | −0.003 (2) | 0.002 (2) | −0.002 (2) |
| O9 | 0.013 (2) | 0.016 (3) | 0.013 (2) | −0.002 (2) | −0.002 (2) | −0.001 (2) |
| O10 | 0.013 (2) | 0.024 (3) | 0.010 (2) | 0.005 (2) | 0.003 (2) | 0.003 (2) |
| O11 | 0.017 (2) | 0.018 (3) | 0.016 (2) | 0.004 (2) | 0.007 (2) | 0.004 (2) |
| O12 | 0.014 (2) | 0.016 (3) | 0.015 (2) | 0.000 (2) | −0.004 (2) | −0.001 (2) |
| As1—O1 | 1.677 (5) | Mo2—O12 | 1.715 (6) |
| As1—O2 | 1.695 (5) | Mo2—O7 | 1.987 (5) |
| As1—O3 | 1.698 (5) | Mo2—O4iii | 2.033 (5) |
| As1—O4 | 1.704 (5) | Mo2—O2 | 2.153 (5) |
| As2—O5 | 1.669 (5) | Mo2—O1iv | 2.311 (5) |
| As2—O6 | 1.673 (5) | Li1—O9 | 1.98 (2) |
| As2—O8 | 1.690 (5) | Li1—O5v | 2.01 (2) |
| As2—O7 | 1.699 (5) | Li1—O12vi | 2.07 (2) |
| Mo1—O9 | 1.716 (6) | Li1—O8vi | 2.08 (2) |
| Mo1—O10 | 1.717 (6) | Li1—O6i | 2.18 (2) |
| Mo1—O3 | 1.958 (5) | Li2—O1 | 1.93 (2) |
| Mo1—O8i | 2.029 (5) | Li2—O10 | 2.02 (2) |
| Mo1—O6ii | 2.128 (5) | Li2—O2vii | 2.02 (2) |
| Mo1—O5 | 2.194 (5) | Li2—O4viii | 2.19 (2) |
| Mo2—O11 | 1.698 (6) | Li2—O12ix | 2.23 (2) |
| O1—As1—O2 | 110.5 (3) | O8i—Mo1—O6ii | 80.9 (2) |
| O1—As1—O3 | 110.9 (3) | O9—Mo1—O5 | 162.2 (2) |
| O2—As1—O3 | 109.8 (3) | O10—Mo1—O5 | 89.8 (2) |
| O1—As1—O4 | 114.3 (3) | O3—Mo1—O5 | 92.1 (2) |
| O2—As1—O4 | 106.7 (3) | O8i—Mo1—O5 | 74.4 (2) |
| O3—As1—O4 | 104.3 (3) | O6ii—Mo1—O5 | 72.0 (2) |
| O5—As2—O6 | 109.4 (3) | O11—Mo2—O12 | 103.3 (3) |
| O5—As2—O8 | 108.5 (3) | O11—Mo2—O7 | 97.2 (2) |
| O6—As2—O8 | 110.7 (3) | O12—Mo2—O7 | 97.1 (2) |
| O5—As2—O7 | 107.2 (2) | O11—Mo2—O4iii | 94.3 (2) |
| O6—As2—O7 | 116.2 (3) | O12—Mo2—O4iii | 89.5 (2) |
| O8—As2—O7 | 104.5 (3) | O7—Mo2—O4iii | 165.0 (2) |
| O9—Mo1—O10 | 101.7 (3) | O11—Mo2—O2 | 99.1 (2) |
| O9—Mo1—O3 | 100.8 (3) | O12—Mo2—O2 | 157.3 (2) |
| O10—Mo1—O3 | 92.4 (2) | O7—Mo2—O2 | 83.8 (2) |
| O9—Mo1—O8i | 89.9 (2) | O4iii—Mo2—O2 | 84.9 (2) |
| O10—Mo1—O8i | 101.8 (2) | O11—Mo2—O1iv | 172.5 (2) |
| O3—Mo1—O8i | 160.1 (2) | O12—Mo2—O1iv | 83.9 (2) |
| O9—Mo1—O6ii | 97.7 (2) | O7—Mo2—O1iv | 83.6 (2) |
| O10—Mo1—O6ii | 160.3 (3) | O4iii—Mo2—O1iv | 83.8 (2) |
| O3—Mo1—O6ii | 81.1 (2) | O2—Mo2—O1iv | 73.6 (2) |
| Symmetry codes: (i) −x+2, y−1/2, −z+2; (ii) x−1, y, z; (iii) −x+1, y+1/2, −z+1; (iv) −x+2, y+1/2, −z+1; (v) −x+1, y−1/2, −z+2; (vi) x−1, y−1, z; (vii) −x+2, y−1/2, −z+1; (viii) −x+1, y−1/2, −z+1; (ix) x, y−1, z. |
Experimental details
| Crystal data | |
| Chemical formula | LiMoO2(AsO4) |
| Mr | 273.80 |
| Crystal system, space group | Monoclinic, P21 |
| Temperature (K) | 298 |
| a, b, c (Å) | 5.1173 (7), 8.561 (2), 10.309 (1) |
| β (°) | 94.63 (1) |
| V (Å3) | 450.16 (13) |
| Z | 4 |
| Radiation type | Mo Kα |
| µ (mm−1) | 10.15 |
| Crystal size (mm) | 0.16 × 0.08 × 0.04 |
| Data collection | |
| Diffractometer | Enraf-Nonius CAD-4 diffractometer |
| Absorption correction | ψ scan (North et al., 1968) |
| Tmin, Tmax | 0.343, 0.676 |
| No. of measured, independent and observed [I > 2σ(I)] reflections | 1801, 1385, 1325 |
| Rint | 0.030 |
| (sin θ/λ)max (Å−1) | 0.703 |
| Refinement | |
| R[F2 > 2σ(F2)], wR(F2), S | 0.025, 0.064, 1.09 |
| No. of reflections | 1385 |
| No. of parameters | 164 |
| No. of restraints | 1 |
| Δρmax, Δρmin (e Å−3) | 1.38, −1.72 |
Computer programs: CAD-4 EXPRESS (Duisenberg, 1992; Macíček & Yordanov, 1992), CAD-4 EXPRESS, XCAD4 (Harms & Wocadlo, 1995), SHELXS86 (Sheldrick, 1990), SHELXL97 (Sheldrick, 1997), DIAMOND (Brandenburg, 1998), SHELXL97.
| As1—O1 | 1.677 (5) | Mo2—O12 | 1.715 (6) |
| As1—O2 | 1.695 (5) | Mo2—O7 | 1.987 (5) |
| As1—O3 | 1.698 (5) | Mo2—O4iii | 2.033 (5) |
| As1—O4 | 1.704 (5) | Mo2—O2 | 2.153 (5) |
| As2—O5 | 1.669 (5) | Mo2—O1iv | 2.311 (5) |
| As2—O6 | 1.673 (5) | Li1—O9 | 1.98 (2) |
| As2—O8 | 1.690 (5) | Li1—O5v | 2.01 (2) |
| As2—O7 | 1.699 (5) | Li1—O12vi | 2.07 (2) |
| Mo1—O9 | 1.716 (6) | Li1—O8vi | 2.08 (2) |
| Mo1—O10 | 1.717 (6) | Li1—O6i | 2.18 (2) |
| Mo1—O3 | 1.958 (5) | Li2—O1 | 1.93 (2) |
| Mo1—O8i | 2.029 (5) | Li2—O10 | 2.02 (2) |
| Mo1—O6ii | 2.128 (5) | Li2—O2vii | 2.02 (2) |
| Mo1—O5 | 2.194 (5) | Li2—O4viii | 2.19 (2) |
| Mo2—O11 | 1.698 (6) | Li2—O12ix | 2.23 (2) |
| Symmetry codes: (i) −x+2, y−1/2, −z+2; (ii) x−1, y, z; (iii) −x+1, y+1/2, −z+1; (iv) −x+2, y+1/2, −z+1; (v) −x+1, y−1/2, −z+2; (vi) x−1, y−1, z; (vii) −x+2, y−1/2, −z+1; (viii) −x+1, y−1/2, −z+1; (ix) x, y−1, z. |
 Subscribe to Acta Crystallographica Section C: Structural Chemistry
Subscribe to Acta Crystallographica Section C: Structural Chemistry
The full text of this article is available to subscribers to the journal.
- Information on subscribing
- Sample issue
- Purchase subscription
- Reduced-price subscriptions
- If you have already subscribed, you may need to register

 journal menu
journal menu

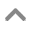



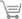
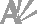

![[Figure 1]](https://journals.iucr.org/c/issues/2004/08/00/dn1050/dn1050fig1thm.gif)
![[Figure 2]](https://journals.iucr.org/c/issues/2004/08/00/dn1050/dn1050fig2thm.gif)
![[Figure 3]](https://journals.iucr.org/c/issues/2004/08/00/dn1050/dn1050fig3thm.gif)




L'élaboration de nouveaux matériaux pouvant être potentiellement des conducteurs ioniques (Yao & Kummer, 1967; Hong, 1976), des échangeurs d'ions (Crosnier et al., 1991; Troup & Clearfield, 1977), utilisés en catalyse hétérogène (Lii et al., 1987) ou bien comme produits d'intercalation (Guesdon et al., 1990), a conduit à s'intéresser aux composés à charpente ouverte formée d'octaèdres et à charpente mixte constituée d'octaèdres et de tétraèdres. En effet, de nombreux travaux relatifs à la découverte de certains de ces nouveaux matériaux dits `électroniques' doués en particulier de conductivité (Guyomard & Tarascon, 1994; Broussely et al., 1993; Delmas et al., 1999), ont motivé la recherche et ont conduit à un formidable développement des équipements électroniques portables.
C'est dans ce cadre que nous avons entrepris l'étude des oxydes mixtes au lithium. Un examen bibliographique ne révèle dans le système Li—Mo—As—O qu'un seul composé de formulation LiMoO2AsO4 (Linnros, 1970). Nous avons alors poursuivi l'investigation de ce système. Plusieurs tentatives de préparations de composés au lithium dans la zone acide du diagramme Li—Mo—As—O par réaction à l'état solide, ont conduit vers le même matériau LiMoO2AsO4. Ce travail montre que cette phase présente un large domaine de stabilité. Cependant une nouvelle forme allotropique, que nous appellerons β-LiMoO2AsO4 a été caractérisée et fait l'objet de la présente étude structurale.
La structure du composé étudié a été résolue dans le groupe spatial non centosymétrique (P21). Une tentative d'affinement dans le groupe d'espace P21/m conduit à un facteur de reliabilité non pondéré élevé (19%) et à certaines distances inter-atomiques anormalement courtes.
La structure du composé β-LiMoO2AsO4 est constituée à partir d'octaèdres MoO6 et de tétraèdres AsO4 partageant des sommets. L'unité asymétrique Mo2As2O14 est cyclique. Elle est formée par deux octaèdres MoO6 et deux tétraèdres AsO4 (Fig. 1). Quatre unités Mo2As2O14 se connectent par mize en commun de sommets, dans les directions [011] e t [011] pour former des cycles à huit polyèdres limitant de larges sections de tunnels dans le plan (100). De plus, par formation de ponts Mo—O—As selon la direction [100] ces unités conduisent à une charpente tridimensionnelle laissant libre des canaux, parallèles à [100], logeant les cations Li+ (Fig. 2).
Les atomes d'arsenic, de molybdène et de lithium forment respectivement avec les atomes d'oxygènes des liaisons As—O, Mo—O et Li—O conformes à celles rencontrées dans la littérature (Zid & Jouini, 1996, 1999; Linnros, 1970). Au sein des octaèdres MoO6, on relève deux liaisons Mo═O courtes caractéristiques des groupements molybdényls MoO2. Le calcul des différentes valences des liaisons, utilisant la formule empirique de Brown (Brown & Altermatt, 1985) et développée par O'Keeffe (Brese & O'Keeffe, 1991), conduit aux valeurs des charges des ions Mo1 (6,03), Mo2 (5,90), As1 (4,95), As2 (5,07), Li1 (1,00) e t Li2 (0,99) conformes aux degrés d'oxydation attendus.
La comparaison de la structure étudiée avec celle de la forme connue du composé isoformulaire LiMoO2AsO4 (Linnros, 1970), que nous appellerons forme α, montre que ces deux composés appartiennent à une classe non centrosymétrique. Mais la forme α est orthorombique (Pn21a). Signalons aussi que, dans la charpente anionique du composé α-LiMoO2AsO4, les unités (MoO2AsO4)− se connectent entre elles pour former des cycles à six polyèdres au centre desquels réside un seul type d'ion Li+, contre des cycles à huit polyèdres dans la forme β. Il en résulte un élargissement de la section des canaux de la forme β. En effet les distances O—O les plus longues et les plus courtes dans ces canaux sont respectivement égales à 7,34 (1) e t 3,40 (3) Å dans la forme β et à 6,36 (2) e t 2,87 (2) Å dans la forme α, ce qui devrait théoriquement favoriser la mobilité ionique des ions Li+ dans la forme β (Fig. 3). Cependant Li1 et Li2, occupent des positions excentrées dans les tunnels de manière à se trouver aux centres d'une bipyramide à base triangle et d'une pyramide à base carré respectivement. Les fenêtres de sortie de ces polyèdres sont assez étroites, ce qui constitue un facteur défavorable à la conductivité.
La comparaison de la structure du composé β-LiMoO2AsO4 avec celles rencontrées dans la littérature et renfermant la même unité cyclique M2X2O14 (M est Mo ou V et X est P ou As) montre une filiation structurale avec les composés à charpente bidimensionnelle KMo(H2O)O2PO4 (Millini & Carati, 1995) et β-VO(HPO4)2H2O (Le Bail, 1989) d'une part et ceux à charpente tridimentionnelle de formulation AMoO2XO4 (A est Na, K ou Rb et X est P ou As) (Zid & Jouini, 1996, 1999; Peascoe & Clearfield, 1991; Kierkegaard, 1962) et B(MoO2)2(XO4)2 (B est Ba, Pb et Sr) (Masse et al., 1985; Hsu & Wang, 1999) d'autre part.
En effet, on peut considérer que par l'élimination des molécules d'eau existant entre les couches et la jonction de ces dernières par partage de sommets entre octaèdres et tétraèdres, il y a passage de la charpente bidimensionnelle des structures des composés hydratés cités précédemment à une charpente tridimensionnelle similaire à celle existant dans les composés de formulation analogue AMoO2XO4 (A est Li, Na, K ou Rb et X est P ou As), le composé du titre inclus.
La comparaison avec la forme β du monophosphate PbVO2PO4 (Borel et al., 2000) montre que la structure de ce dernier présente le même type d'unités cycliques V2P2O14 qui se connectent pour former des couches infinies similaires à celles rencontrées dans le composé étudié mais elles ne sont pas directement reliées entre elles. La jonction des couches (V2P2O14)∞ se fait par l'intermédiaire de deux types de tétraèdres VO4 et PO4 dans la forme β-PbVO2PO4.
Le composé β-LiMoO2AsO4, appartenant à une classe non centrosymétrique et renfermant des groupements molybdenyls MoO2, peut manifester des propriétés d'optique non linéaire (Stucky et al., 1989; Crosnier et al., 1990) et notamment de luminescence (Hazenkamp Strijbosch & Blasse, 1992; Hazenkamp Voogt & Blasse, 1992).